mashbean 黃豆泥
mashbean.eth
豆泥的以太坊地址: mashbean.eth
狀態: 未簽名
0x67af431742cbb6997b576f1bbfad93a671431cc9522ed77dfd9f692f3674b5e6
已簽名表示這篇文章已建立獨特的身分證字號(內容雜湊,contentHash)並且由豆泥簽署認證,簽署是採用以太坊區塊鏈的豆泥專用地址(signer.mashbean.eth)。只要內容一經修改,就會需要重新驗證換發新的身分證字號。但豆泥不是每天都在公所上班,所以偶爾會慢一點認證。
本文探討FDA加速核准阿茲海默症藥物Aducanumab的爭議背景,並闡述阿茲海默症診斷標準從症狀導向轉向分子病理導向的研究框架,預示未來治療策略與疾病認知的重大變革。
〖失智症診斷治療的典範轉移,核子醫學科位處戰略關鍵〗
六月七日一則新聞震撼全球,一種用於阿茲海默症的 Aducanumab 經美國食品藥物管理局(FDA)核准加速核准(Accelerated approval),這是第一款針對阿茲海默症可能的真正病因進行打擊的藥物。 Aducanumab 的機轉為使用單株抗體來減少腦內 β 類澱粉蛋白的藥物,在這之前,市面上針對阿茲海默症的藥物只能延緩後期症狀,並不能根治。不過當然,Aducanumab 也不能根治阿茲海默症,事實上,到目前為止學術界連阿茲海默症的真正病因都還不清楚。
Aducanumab 並不能被當作失智症的神奇子彈,但說它是進入治療新紀元的黎明號角應不為過。
核子醫學科的老師看到新聞很興奮,於是派我在期刊會議上面報一篇用來診斷阿茲海默症分子影像(Amyloid PET)的新文章,而該文章使用的診斷性藥物與技術,北榮也有使用它進行研究。
身為吃瓜群眾,整理資料的過程具有學術娛樂價值,兩個原因:藥物上市爭議與疾病/治療架構可能怎麼改變。以下將剔除數據與專有名詞,以娛樂向的口吻討論整件事。
*
藥物上市爭議
Aducanumab 的藥物在批准的過程極具爭議性,該藥物的兩個大型第三期臨床試驗(ENGAGE [NCT02477800], EMERGE [NCT02484547])其實在 2019 年 3 月因為未達目標(prespecified futility criteria)而停止,在該年 9 月又因為重新分析結果發現部分有效而重新啟動。且最後的結果兩者是互相衝突的,只有在高劑量組別顯示一致的治療效果,FDA 中的諮詢委員會以幾乎是全票反對的票數反對其藥物效果。搞到後來外部諮詢委員辭職了一大半以示抗議,其中德高望重的神經系統諮詢委員會前主席 G. Caleb Alexander 藥物上市的前一個月還寫了一篇措辭非常強烈的觀點投書到 JAMA 批判 FDA 的決定,質疑 FDA 從此大開方便之門,鑄下不良先例。
於此同時 Biogen 股價已經一飛沖天。
總之接下來的看點是上市後 Aducanumab 的表現會不會被 FDA 打回票,與其產生龐大的市場利潤。
另外,適用 Aducanumab 的對象是輕度認知障礙的病人。但輕度認知障礙的病人並不一定符合阿茲海默症的定義,如何早期偵測早期診斷,繼而進入治療就是接下來的臨床議題。
*
疾病/治療架構的典範轉移
雖然前面在神經科待了兩個月,甚至還跟到專精失智症的老師,但我對失智症乃至於阿茲海默症的診斷治療仍然非常陌生,所以重新回去審視診斷標準。
到目前為止,阿茲海默症的絕對診斷還是需要靠屍體解剖,從顯微鏡看大腦有無類澱粉沈積來做判斷,但是診斷是用來治療的,人死了就沒有意義。所以國際間的診斷標準目前以症狀為主。
以美國國家級機構 National Institute on Aging - Alzheimer Association (以下簡稱 NIA-AA)為例,阿茲海默症的定義總共有三個版本。第一版是 1984 年,過了 27 年該組織在 2011 推出第二版,兩個版本對於阿茲海默症的定義都是以臨床症狀為診斷核心, 2011 年改版,分出疾病前期與輕微認知障礙的期別,還有承認分子病理證據能增加符合疾病診斷的可信度。
隨著診斷工具進步,學術界普遍認為失智症是一種蛋白質病變,不同蛋白質病變的證據可以對應到不同失智症表現。阿茲海默症相關的蛋白質病變可能牽涉到 β 類澱粉蛋白與磷酸化的 p-Tau 蛋白。核子醫學科的特殊檢查 Amyloid PET(如以 [18F]Flurobetaben 的藥物進行正子斷層造影)可以不必屍解就可以看到蛋白質病變在腦袋裡的分布狀態,同時間核醫也在發展看 Tau 蛋白沉積的 Tau PET;另外,做腰椎穿刺也可以藉由腦脊隨液的蛋白質比例間接判斷大腦病態蛋白沈積程度。
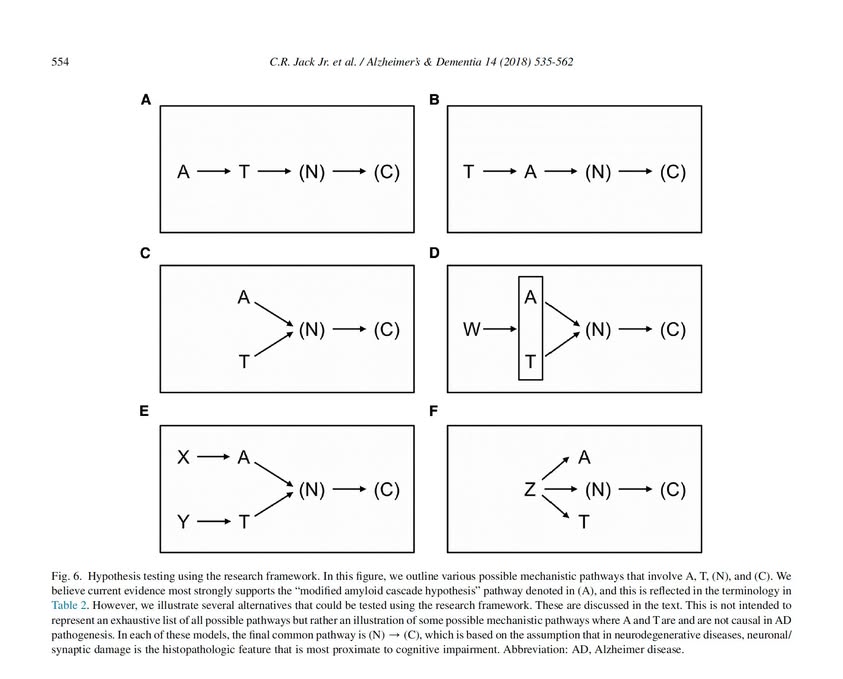
因應診斷工具的強化,NIA-AA 在 2018 年推出了研究框架版本(Reseacr framework),這個版本推翻 2011 年的定義,將阿茲海默症定義為「分子病理導向」的疾病,而非「症狀導向」的疾病。原先的定義歸納進臨床症候群(Azheimer’s clinical syndrome)。同時間,NIA-AA 2018 將分子病理證據作出更細緻的分期,有如癌症的 TNM 分類(tumor / lymph node / metastasis),Reseacrh framework 也有 AT(N) 分類,分別為 A = Amyloid; T = Tau; N = Neuronal injury (神經損傷,括號是因為該項並非絕對要素)。A 與 T 皆可以透過 PET 或腰椎穿刺來得到答案,N 可以做核子醫學科的 [18F]FDG-PET 正子斷層造影看大腦葡萄糖代謝狀態。當有取得類澱粉沈積與 tau 蛋白病變證據的狀態下才能被稱之為阿茲海默症。同一篇指引同時列舉了 A, T, N 與 C (Clinical 臨床症狀)之間可能的因果關係(如圖),讓研究者可以依循架構來印證阿茲海默症到底是怎麼來的。
當然該指引強調這個分類是用於研究用途,並不能拿來臨床使用。但這個分類顛覆了我以前國考背的「阿茲海默症要兩個認知領域受損才符合條件」。時代的進步讓疾病的定義框架開始轉變,醫學科技躍進的巨輪正在碾壓我的臨床知識。
*
阿茲海默症的病因雖然還沒有被破解,但阿茲海默症的整體架構正在從症狀框架轉移到病理框架,這是一場牽涉利益巨大的典範轉移。
再加上失智症盛行率之廣,其治療策略、疾病認知的改變將進入主流文化,影響整個世代,如同突飛猛進的癌症治療一樣。
有沒有可能在我成為老頭子的時代,在還沒有認知障礙之前,就先被診斷出有壞蛋白在腦子裡堆積,健保馬上投與藥物/微型機器清除潛在風險,整個治療邏輯完全不同,如同日本動畫心靈判官(PsychoPass)的概念,在還沒犯罪之前就先被移除。 2011 年與 1984 年只過了 27 年,整個定義因應時空變化出現巨大改變,再過 30 年科技會進步到什麼樣子實在很難想像。
有沒有可能以後我直接在尚未出現的核醫科門診直接做檢查,同時過磅空做完三合一正子斷層檢查 Amyloid PET、Tau PET、FDG PET/MRI 之後機器自動診斷有沒有符合阿茲海默症治療的適應症,若符合可以直接領藥服用(每一個檢查現在看起來超級燒錢的!)。整個科技進步的日程可能還要非常久,但核醫不是很擅長曠日費時的觀察研究嗎?看看日本核爆對於人體的影響,就可以知道時間跨度多長。
在「分子病理」的治療框架下,人們會對疾病的認知會產生什麼改變呢?
以前對於疾病的想像是對症下藥,有病就要醫,所以有神奇子彈的迷信。現在大家知道並不是每一種病都有特效藥可以治療。大眾開始對疾病有時序上的認知,疾病不能拖,前後嚴重度有差別,「早期發現,早期治療」琅琅上口。
在未來「分子診斷、分子治療」進入大眾認知的時代,「沈默的根治」或許會成為主流,拒敵於千里之外,如此概念感覺與目前流行的預防保健非常契合。
*
結論是阿茲海默症之謎的破解過程中,將連帶影響人類對疾病的認知,不論是診斷工具進步還是大量新藥上市都會造成影響,畢竟阿茲海默症實在太知名了。而我們有幸身處於科技進步的時代之中。
我以前認為機器本位的科別仍然會有長足的發展空間,如微創手術、影像診斷機器、迴旋加速器、自動化可能性高的科別等等,如今仍抱持著一樣的信仰。
感謝核醫科讓我有時間做報告做夢。
*
(圖為阿茲海默症可能的致病機轉,最主流的假說是左上角的 Amyloid Cascade Hypothesis:A 類澱粉 -> T Tau 蛋白 -> N 神經損傷 -> C 臨床症狀)
圖片來源:NIA-AA Research Framework: Toward a biological definition of Alzheimer’s disease, Alzheimer’s & Dementia, 14 (2018) 535-562